「多原子イオン,電子配置」に関するQ&A

覚えるべきイオンの数なんてまだ少ない方ですし、知識はちゃんと後で付いてきます。 この考え方で、多原子イオン価数は求まります。 所長 「ちょっと待て、ローザ!今のやりとり、まるでイオンだな!」 ローザ 「イオン?スマホやノートパソコンのバッテリーに使われている『リチウムイオン電池』のイオンってこと?」 所長 「そうだ。
13
覚えるべきイオンの数なんてまだ少ない方ですし、知識はちゃんと後で付いてきます。 この考え方で、多原子イオン価数は求まります。 所長 「ちょっと待て、ローザ!今のやりとり、まるでイオンだな!」 ローザ 「イオン?スマホやノートパソコンのバッテリーに使われている『リチウムイオン電池』のイオンってこと?」 所長 「そうだ。
131 分子が存在する場合でも、種々の理由によって、分子式で表すのが困難な場合には組成式で表します。 他のイオンの場合には、内側にも電子格殻が存在しますので、原子格がむき出しになることはありません。
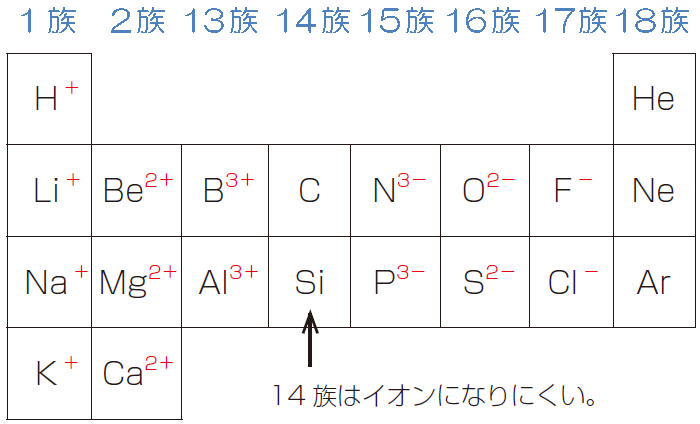
硝酸イオンNO3-は、Nの価電子が5で、あと3こ電子を受け取りたいので、Oが3つだから、Oから1つづつ受け取って、OもNから1つづつ受けとって、(O1つにつき、電子1つNから受け取って)でも、Oは本当は、2つ受け取って、Mカクを、8にしたい・・、しかし、1つうけとり、7で、そのOが3つだから、NO3は、マイナス3価になるのではないのでしょうか? 基本的に考え方がちがうのでしょうか? よろしくお願いいたします。 有効数字、確かによくわからない考え方ですよね。
図 1 に、各セルガスモードを使用して測定された、各マトリクス内のクロムの見かけの濃度 質量 52 の優先同位体で測定 を示します。 水和された銅イオン、アンモニアが配意した銅イオンもはっきりとした色の違いがあります。
(私も習った当初はちんぷんかんぷんでした) そもそも、 「有効数字とはどんな時に使う物なのか?」とか、 「有効数字は何のために考えるのか?」がわからないと、 ただ、「考えるのがとても厄介なよくわからない数字」になってしまうと思います。 A ベストアンサー こんにちは。
14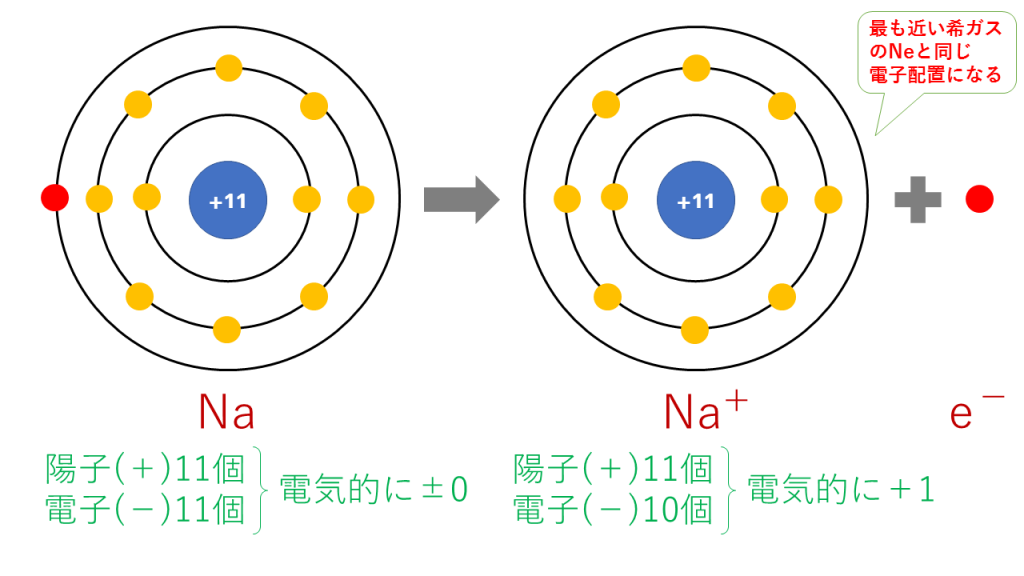
多原子イオンはそのような原子の集団が全体として 電子を得たり失ったりしてイオンになったものです。